Autor : Óscar López Manzanero
4º Curso de Medicina grupo "C" (curso 2024/25)
Código de trabajo : 2415-OLM
Para aproximarnos al diagnóstico del SSD podemos realizar varias pruebas (5):
INTRODUCCIÓN
El síndrome de Schwachmann-Diamond (SSD) es un trastorno multisistémico poco frecuente que se caracteriza por un cuadro neutropénico crónico y generalmente leve, insuficiencia pancreática exocrina asociada a esteatorrea y retraso del crecimiento, displasia esquelética que hace que quienes lo padezcan presenten una estatura baja y un mayor riesgo de desarrollar aplasia medular o leucemia. El pronóstico es variable. Las complicaciones con peor pronóstico son la aplasia medular y la transformación leucémica (1).
EPIDEMIOLOGÍA
Se trata de un trastorno que fue descrito por primera vez en 1964, y consiste en un síndrome hereditario, autosómico recesivo, que se da en uno de cada cien mil nacimientos. Es ligeramente más prevalente en la mujer. Y es la segunda causa más frecuente de insuficiencia pancreática exocrina en la infancia, por detrás de la fibrosis quística (2).
ETIOLOGÍA
Recientemente se ha descubierto la influencia del gen SBDS como responsable del síndrome. Se ha visto que mutaciones de este gen en el brazo largo del cromosoma 7, en posición 11,21 (7q11.21) codifican una proteína de función todavía desconocida, pero que se expresa activamente en casi todas las células del organismo. Parece participar en el procesamiento del ARN y en la constitución de los ribosomas.
Se han encontrado más de 20 mutaciones responsables del SSD. La mayoría de ellas se producen como resultado de un intercambio de material genético entre el gen SBDS y pseudogenes del ADN localizados cerca del cromosoma 7. Las dos mutaciones más estudiadas producen cambios en los nucleótidos del gen: 258 + 2T>C y 183-184TA>CT. Estos cambios frenan prematuramente la codificación de la proteína. Como ya hemos comentado, se trata de un fenómeno autosómico recesivo; por tanto, deben estar afectadas ambas copias del gen (3).
CLÍNICA
Los síntomas de esta patología pueden variar de un niño a otro, pero como ya se ha comentado, afectan a varios aparatos y sistemas. Los síntomas y signos más característicos son los siguientes: (4)
- Alteraciones pancreáticas. Se observan en cuantías variables, como resultado de falta de desarrollo de los acinos pancreáticos.
- Malabsorción. Aparece en el 90% de los pacientes y se manifiesta mediante estados carenciales de vitaminas liposolubles y de otros macronutrientes, debido a la insuficiencia de secreción pancreática.
- Diarrea. Suele presentarse de manera crónica y acompañada de esteatorrea, por la falta de digestión de las grasas.
- Alteraciones hepáticas. Elevación de transaminasas.
- Dolor y distensión abdominal. Relacionado también con la insuficiencia pancreática.
- Infecciones frecuentes. Como consecuencia de la neutropenia, aumenta la predisposición del paciente de padecer infecciones.
- Anormalidades del esqueleto y crecimiento reducido. El 50% de los pacientes presentan disostosis metafisaria que afecta principalmente a la cabeza del fémur, aunque ocasionalmente es asintomática.
- Piel pálida.
- Falta de energía (astenia).
- Equimosis y erupciones cutáneas.
- Sangrado de mucosas.
- Anemia y trombocitopenia. Pueden aparecer en un 30% de los casos.
- Alteraciones cerebrales y fallos cognitivos.
DIAGNÓSTICO
Para aproximarnos al diagnóstico del SSD podemos realizar varias pruebas (5):
EVALUACIÓN CLÍNICA. ANAMNESIS Y EXPLORACIÓN FÍSICA
Localizar signos y síntomas característicos de esta patología.
ANALÍTICA DE SANGRE. HEMOGRAMA
Evaluación de eritrocitos, leucocitos y plaquetas. Para que se cumpla con el diagnóstico tiene que haber citopenia crónica, manifestada mediante al menos una de las siguientes: (4)
- Neutrófilos < 1,5 x 103
- Hb < a 2 desviaciones estándar de la media ajustada para la edad.
- Trombocitopenia < 150 x 103
PRUEBAS DE FUNCIÓN PANCREÁTICA
PRUEBAS DIRECTASSe basan en la recogida del jugo pancreático tras la estimulación para determinar la actividad del páncreas.Se usa principalmente la prueba de la secretina-ceruleína. Al paciente, en ayunas, se le coloca una sonda de doble luz que succionará evitando la mezcla de contenido gástrico y duodenal. Seguidamente, se administran de manera intravenosa ceruleína y secretina, que estimulan la secreción de enzimas pancreáticas y agua y bicarbonato, respectivamente. La secreción pancreática basal se recolecta y se cuantifican sus componentes (6).PRUEBAS INDIRECTAS
Estas pruebas consisten en valorar la función pancreática mediante la determinación de enzimas pancreáticas en suero o heces, o bien evaluando la capacidad de digestión de la glándula durante las comidas (7).
PRUEBAS DE IMAGEN
Es necesario realizar pruebas de imagen radiológicas con el fin de detectar anomalías óseas. Importante incluso aunque no haya malformaciones visibles, pues recordemos que hay pacientes que pueden presentar disostosis metafisaria asintomática. También es importante el uso de ecografía para detectar anomalías pancreáticas y hepáticas.
TEST DEL SUDOR
Diagnóstico diferencial con la fibrosis quística.
BIOPSIA Y ASPIRACIÓN DE MÉDULA ÓSEA
Confirmatoria.
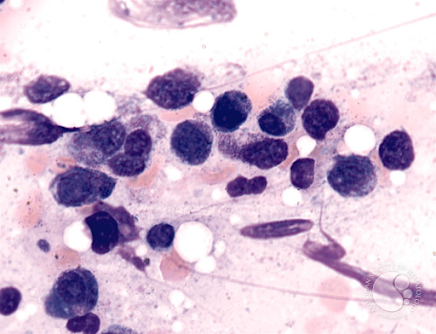
Imagen 1. Médula ósea en Síndrome de Schwachmann-Diamond-Oski.
Obtenida de: https://www.femexer.org/9416/sindrome-de-shwachman-diamond/
PRUEBA DE GRASA EN HECES: VAN DE KAMER
Analizar el grado de malabsorción y, así, el grado de insuficiencia pancreática.
PRUEBAS GENÉTICAS
Con el fin de detectar mutaciones en el gen SBDS.
DIAGNÓSTICO DIFERENCIAL
El diagnóstico diferencial incluye las siguientes patologías:
FIBROSIS QUÍSTICA
Es una enfermedad hereditaria causada por un gen mutado (CFTR) que provoca alteraciones en los canales de cloro, provocando un cambio en la secreción mucosa, que se vuelve más espesa, afectando principalmente a las vías respiratorias, pero también a otros órganos, especialmente en el tracto digestivo, y concretamente al páncreas, causando una insuficiencia pancreática similar a la del SSD (8).
SÍNDROME DE PEARSON
Se trata de una alteración de la fosforilación oxidativa mitocondrial que se produce por una deleción de ADN mitocondrial, caracterizada por anemia hiporregenerativa en la que los precursores hematopoyéticos presentan vacuolas en su citoplasma. Se produce además acidosis láctica y disfunción multiorgánica, como insuficiencia pancreática exocrina y tubulopatía renal. Los síntomas de los pacientes con esta enfermedad incluyen retraso en el crecimiento, afectación neurológica y afectación gastrointestinal (vómitos, diarrea…) (9).
ANEMIA DE FANCONI
Enfermedad hereditaria, autosómica recesiva, de muy baja frecuencia entre la población. Se caracteriza por insuficiencia medular progresiva, con anemia, leucopenia y trombocitopenia, además de malformaciones congénitas y alta predisposición tumoral. Entre los síntomas principales, encontramos retraso del crecimiento, malformaciones renales, gastrointestinales, cardiacas, genitales y urinarias, y alteraciones esqueléticas: cabeza, ojos y boca pequeños; entre otra sintomatología (10).
ANEMIA DE BLACKFAN-DIAMOND
Trastorno en el que la médula ósea no es capaz de producir suficientes eritrocitos. Se producen alteraciones esqueléticas (pulgares deformes o con tres falanges es algo bastante típico) y otras anomalías físicas. Presentan un riesgo elevado de desarrollar leucemias y osteosarcoma. Se debe, al igual que el SSD, a la mutación de genes que modifican la síntesis de los ribosomas (11).
TRATAMIENTO
El manejo debe ser multidisciplinar, e incluir a un hematólogo, un gastroenterólogo, un nutricionista, un endocrinólogo y un ortopedista.
MANEJO HEMATOLÓGICO
Prevención de infecciones. Como consecuencia de la neutropenia, estos pacientes pueden presentar infecciones con más facilidad que la población sin la enfermedad. Convendría administrar antibióticos profilácticos.
Factores de crecimiento hematopoyético. Se puede usar Filgastrim (G-CSF) u otros fármacos para estimular la producción de los neutrófilos.
Transplante de células madre hematopoyéticas. Actualmente, es el único tratamiento curativo.
MANEJO NUTRICIONAL Y PANCREÁTICO
Terapia hormonal pancreática. La administración de enzimas pancreáticas puede facilitar la digestión de los alimentos, evitando síntomas como la esteatorrea o la diarrea.
Soporte nutricional. Una dieta equilibrada y con suplementos de vitaminas liposolubles ayudarían a tratar el déficit nutricional.
MANEJO DEL ESǪUELETO Y DEL CRECIMIENTO
Intervenciones ortopédicas. El control de la salud ósea y las intervenciones oportunas ante la presencia de anomalías esqueléticas mejoran la calidad de vida del paciente.
Terapia con hormona de crecimiento. Se usa para abordar el retraso del crecimiento (12).
CASO CLÍNICO
Para terminar, me gustaría hacer referencia a un caso clínico, ya que es así como mejor se verá representada esta patología. El caso clínico fue presentado por la Asociación Española de Pediatría, y es el siguiente: (13)
“Un lactante de 14 meses es remitido a nuestro servicio para estudio de una hipertransaminasemia y un estancamiento ponderal desde los 9 meses de edad. El niño no presenta ningún antecedente familiar ni personal de interés. El peso al nacer fue de 3.390 g y la talla de 51 cm. Ha presentado un adecuado desarrollo ponderoestatural hasta los 9 meses de edad, momento en el que empezó a presentar 4-5 deposiciones por día, pegajosas y de olor rancio junto con un estancamiento ponderoestatural”.
Tras analizar el cuadro clínico, su pediatra le realizó una analítica en la que solo destacó una GOT de 464 U/l y una GPT de 514 U/l. Esta hipertransaminemia persistió durante más de tres meses, por lo que el lactante fue estudiado. En la exploración física destacaba un aspecto microsómico armónico, con un peso y una talla por debajo del percentil 3. El resto de la exploración fue normal. Se le realizó una serie de exámenes complementarios:
- Hemograma: leucocitos 8.400 (N, 16 %; L, 77 %; M, 5,8 %), hematocrito 34,6 %, hemoglobina 11,6 g/dl y 313.000 plaquetas.
- Bioquímica general: GOT, 417 U/l; GPT, 440 U/l; resto normal.
- Test del sudor normal.
- Van de Kamer: sin esteatorrea.
- Elastasa en heces 11,5 μg/g.
- Serologías negativas.
- Ecografía abdominal: hiperdensidad pancreática sugestiva de insuficiencia pancreática exocrina.
Con todo esto, ante la sospecha de un SSD, se realizó un estudio óseo en el que se vio que el niño era heterocigoto con dos mutaciones del gen SBDS (258 + 2T > C/183-184 TA > CT) con lo que confirma el diagnóstico. Luego se estudió que el padre era portador de la mutación 183-184 TA > CT y que la madre era portadora de la mutación 258 + 2T > C.
El niño comenzó tratamiento con terapia sustitutiva de enzimas pancreáticas y vitaminas liposolubles, con lo que mejoró el estado fecal, pero no el desarrollo en la talla ni en el peso, manteniéndose por debajo del percentil 3. La cifra de neutrófilos fue variando llegando hasta 540 neutrófilos.
BIBLIOGRAFÍA
1.- Orphanet: Síndrome de Shwachman-Diamond [Internet]. Disponible en: https://www.orpha.net/es/disease/detail/811
2.- Macipe Costa R, Javierre Miranda E, Lou Francés M, Heredia González S, Calvo Martín M. Síndrome de Shwachman-Diamond. An Pediatr (Barc). 1 de julio de 2006;65(1):79-82.
3.- Pruebas genéticas - Shwachman-Diamond, Síndrome de ..., (Shwachman- Diamond syndrome) - Gen SBDS. - IVAMI [Internet]. Disponible en: https://www.ivami.com/es/pruebas-geneticas-mutaciones-de-genes-humanos-enfermedades-neoplasias-y-farmacogenetica/1042-pruebas-geneticas-shwachman- diamond-sindrome-de-shwachman-diamond-syndrome-gen-i-sbds
4.- Dialnet-SindromeDeSchwachmanDiamond-8876439.pdf. Disponible en: https://dialnet.unirioja.es/descarga/articulo/8876439.pdf
5.- Síndrome de Shwachman-Diamond (SDS) | Hospital Infantil de Boston [Internet]. Disponible en: https://www.childrenshospital.org/conditions/shwachman-diamond- syndrome
6.- Scribd [Internet]. Función Expcrina Pancreatica | PDF | Heces | Páncreas. Disponible en: https://es.scribd.com/document/612007819/Funcion-expcrina- pancreatica
7.- Iglesias-García J. Estudio de la función pancreática exocrina. Gastroenterol Hepatol. 15 de febrero de 2005;28:10-5.
8.- Fibrosis quística: MedlinePlus enciclopedia médica [Internet]. Disponible en: https://medlineplus.gov/spanish/ency/article/000107.htm
9.- Orphanet: Síndrome de Pearson [Internet]. Disponible en: https://www.orpha.net/es/disease/detail/699
10.- Fundación Josep Carreras contra la leucemia [Internet]. La Anemia de Fanconi - Fundación Josep Carreras. Disponible en: https://fcarreras.org/pacientes/enfermedades-hematologicas-ninos/anemia-de- fanconi/
11.- Definición de anemia de Diamond-Blackfan - Diccionario de cáncer del NCI - NCI [Internet]. 2011. Disponible en: https://www.cancer.gov/espanol/publicaciones/diccionarios/diccionario- cancer/def/anemia-de-diamond-blackfan
12.- Síndrome de Shwachman-Diamond: síntomas, causas y complicaciones [Internet]. Disponible en: https://www.medicoverhospitals.in/es/diseases/shwachmandiamond-syndrome/
13.- Macipe Costa R, Javierre Miranda E, Lou Francés M, Heredia González S, Calvo Martín M. Síndrome de Shwachman-Diamond. An Pediatr (Barc). 1 de julio de 2006;65(1):79-82.
No hay comentarios:
Publicar un comentario
Se admiten comentarios que indiquen posibles errores en los textos y/o sugerencias de temas, y/o propuestas de mejoras en el blog y/o dudas sobre la realización de trabajos. Dado que este blog no es un consultorio médico, no se responderán preguntas realizadas con esa finalidad. Los comentarios que se consideren inapropiados, serán eliminados de inmediato, sin ningún tipo de excepción.